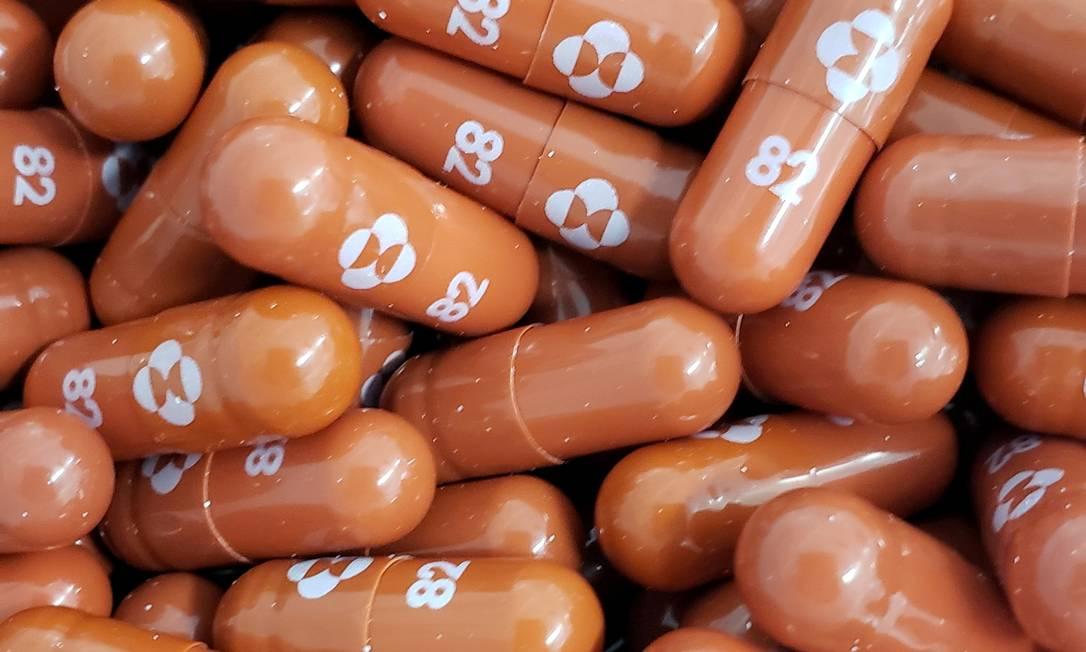
O Reino Unido se tornou o primeiro país a aprovar o uso da pílula Molnupiravir em pacientes com Covid-19. Em comunicado divulgado nesta quinta-feira, a Agência Reguladora de Medicamentos (MHRA, na sigla em inglês) ressaltou que o remédio é "seguro e eficaz para reduzir o risco de admissão hospitalar e morte em pessoas com Covid leve a moderada que sofrem algum risco extra após contrair a doença".
"Hoje é um dia histórico para o nosso país, porque o Reino Unido é agora o primeiro país do mundo a aprovar um antiviral contra a Covid-19 que pode ser tomado em casa. Isso mudará a situação dos mais vulneráveis e imunossuprimidos, que logo poderão receber esse tratamento revolucionário", disse o ministro da Saúde Sajid Javid, em comunicado.
O tratamento foi desenvolvido pela Merck & Co Inc. — MSD no Brasil — em parceria com a Ridgeback Biotherapeutics. O primeiro estudo clínico global com o molnupiravir demonstrou que o antiviral reduziu em aproximadamente 50% o risco de hospitalização ou morte. Os dados demonstraram que 7,3% dos pacientes medicados foram hospitalizados ou morreram, em comparação com 14,1% dos pacientes tratados com placebo. Com base nos dados de sequenciamento viral disponíveis (de aproximadamente 40% dos participantes), molnupiravir demonstrou eficácia consistente contra as variantes Gama, Delta e Mu.
A MSD pediu, em 11 de outubro, uma autorização para uso emergencial à Food and Drug Administration (FDA), agência reguladora dos Estados Unidos. Conselheiros dos EUA se reunirão este mês para votar se o molnupiravir deve ser autorizado.
Também em outubro, a Fiocruz afirmou estar em “conversas avançadas” com a MSD para definir um modelo de cooperação técnica que permita a produção do antiviral contra a Covid-19 pela fundação no Brasil. A MSD incluiu o Brasil em seus estudos de fase 3, que começaram no mês passado no país.
A farmacêutica tem interesse no país. Em nota enviada ao GLOBO, a MSD informou que está mantendo a Anvisa (Agência Nacional de Vigilância Sanitária) "a par sobre os resultados obtidos nas diferentes etapas de estudos clínicos deste medicamento" e que neste momento a fabricante está focada em "terminar de preparar o dossiê com todos os dados e documentos para que o uso emergencial seja analisado pela agência". A empresa informou que "a submissão à Anvisa será solicitada nos próximos dias".
Até o momento, os medicamentos indicados contra a Covid-19 são o remdesivir, antiviral infundido da Gilead Sciences Inc., e o esteróide genérico dexametasona, ambos geralmente administrados apenas quando o paciente já foi hospitalizado.
Produção de genéricos
No último dia 27, a MSD e o Medicines Patent Pool (MPP), uma organização de saúde pública apoiada pelas Nações Unidas, anunciaram a assinatura de um acordo de licenciamento que autoriza outras empresas a produzirem versões genéricas do medicamento.
A licença livre de royalties se aplica a 105 países de baixa e média renda. Ela permite que as fabricantes selecionadas pelo MPP produzam versões genéricas do medicamento, que é uma pílula antiviral desenvolvida em parceria com a Ridgeback Biotherapeutics.